Kemi
Hvordan virker en katalysator?
Jeg skal besvare følgende:
1. Hvad er en katalysator?
Mit svar: en katalysator er et stof, som øger reaktionshastighed uden selv at blive forbrugt. Typisk et fast stof.
2. Hvordan virker katalysatoren?
Her kunne jeg rigtig godt bruge hjælp i form af forklaring med ord og evt et eksempel.
Svar #1
07. maj 2022 af Omar95 (Slettet)
#0Jeg skal besvare følgende:
1. Hvad er en katalysator?
Mit svar: en katalysator er et stof, som øger reaktionshastighed uden selv at blive forbrugt. Typisk et fast stof.
En katalysator er en substans, som øger reaktionshastigheden uden selv at blive omdannet eller forbrugt.
2. Hvordan virker katalysatoren?
Her kunne jeg rigtig godt bruge hjælp i form af forklaring med ord og evt et eksempel.
En katalysator virker som en medspiller (da det hverken er en reaktant eller et produkt) i en reaktion. Katalysatores opgaver er, at få reaktionerne til for at forløbe med lavere aktiveringsenergi, Ea, som gør det muligt for reaktionshastigheden at blive øget. På denne måde bliver det muligt for stoffer, som ikke ville have reageret uden en katalysator, at undgå en reaktion.

Svar #2
08. maj 2022 af lagkage11
#1#0Jeg skal besvare følgende:
1. Hvad er en katalysator?
Mit svar: en katalysator er et stof, som øger reaktionshastighed uden selv at blive forbrugt. Typisk et fast stof.
En katalysator er en substans, som øger reaktionshastigheden uden selv at blive omdannet eller forbrugt.
2. Hvordan virker katalysatoren?
Her kunne jeg rigtig godt bruge hjælp i form af forklaring med ord og evt et eksempel.
En katalysator virker som en medspiller (da det hverken er en reaktant eller et produkt) i en reaktion. Katalysatores opgaver er, at få reaktionerne til for at forløbe med lavere aktiveringsenergi, Ea, som gør det muligt for reaktionshastigheden at blive øget. På denne måde bliver det muligt for stoffer, som ikke ville have reageret uden en katalysator, at undgå en reaktion.
Tusind tak Omar95.
Er en katalysator så "bare" en af de faktorer, der påvirker reaktionshastigheden? Temperatur fx?
Jeg kan godt forstå katalysatorens opgave og hvorfor den er relevant når vi taler reaktionshastighed. Kan du nævne nogle ofte anvendt substanser, som katalysatorer? Føler det giver meget god mening, lige at vide hvad man eksempelvis anvender
Svar #3
08. maj 2022 af Omar95 (Slettet)
#3
Tusind tak Omar95.
Er en katalysator så "bare" en af de faktorer, der påvirker reaktionshastigheden? Temperatur fx?
Nej. Temperatur og lignende er ikke katalysatorer. En substans er et rent stof, ikke et fast stof, temperatur, pH eller lignende.
Jeg kan godt forstå katalysatorens opgave og hvorfor den er relevant når vi taler reaktionshastighed. Kan du nævne nogle ofte anvendt substanser, som katalysatorer? Føler det giver meget god mening, lige at vide hvad man eksempelvis anvender
Kobber er en god katalysator. Spyt er også en katalysator, da spyt indeholder enzymer. Men spyt bruges selvfølgelig mest i biologi.
Svar #4
08. maj 2022 af lagkage11
#3
#3
Tusind tak Omar95.
Er en katalysator så "bare" en af de faktorer, der påvirker reaktionshastigheden? Temperatur fx?
Nej. Temperatur og lignende er ikke katalysatorer. En substans er et rent stof, ikke et fast stof, temperatur, pH eller lignende.
Jeg kan godt forstå katalysatorens opgave og hvorfor den er relevant når vi taler reaktionshastighed. Kan du nævne nogle ofte anvendt substanser, som katalysatorer? Føler det giver meget god mening, lige at vide hvad man eksempelvis anvender
Kobber er en god katalysator. Spyt er også en katalysator, da spyt indeholder enzymer. Men spyt bruges selvfølgelig mest i biologi.
Tusind tak. Vil du måske forklare, hvorfor kobber er en god katalysator og i hvilken sammenhæng?
På forhånd, mange, mange tak
Svar #5
08. maj 2022 af Omar95 (Slettet)
#4Tusind tak. Vil du måske forklare, hvorfor kobber er en god katalysator og i hvilken sammenhæng?
På forhånd, mange, mange tak
Jeg tror ikke man bare kan forklare hvorfor noget er en god katalysator, men f.eks. er kobber en god katalysator for brændselsceller/brændstofceller. Evt. se denne forsøgsvejledning: Eksperiment 1.2: Kobber styrer reaktionen
Svar #6
09. maj 2022 af lagkage11
#5#4Tusind tak. Vil du måske forklare, hvorfor kobber er en god katalysator og i hvilken sammenhæng?
På forhånd, mange, mange tak
Jeg tror ikke man bare kan forklare hvorfor noget er en god katalysator, men f.eks. er kobber en god katalysator for brændselsceller/brændstofceller. Evt. se denne forsøgsvejledning: Eksperiment 1.2: Kobber styrer reaktionen
Okay, det skal jeg måske heller ikke forklare til eksamen - krydser fingre.
Lige til noget helt andet, som du måske kan hjælpe med... Hvorfor er K+ en god tilskuerion til oxidationsmidlet MnO4- ?
Er Kalium med som en oplagt tilskuerion, fordi det er meget villig til at afgive sin elektron med sin lave elektronegativitet, og sin placering langt til venstre i spændingsrækken?
Svar #7
09. maj 2022 af Omar95 (Slettet)
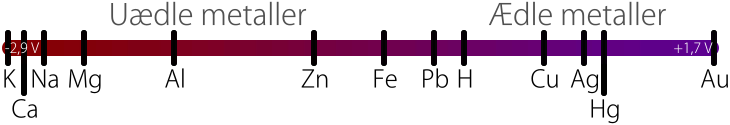
Kalium er meget villig til at afgive én elektron, da den gerne vil ligne Argon. Jeg ved desværre ikke hvorfor det er en god tilskuerion til permanganat.
Skriv et svar til: Hvordan virker en katalysator?
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.






