Kemi
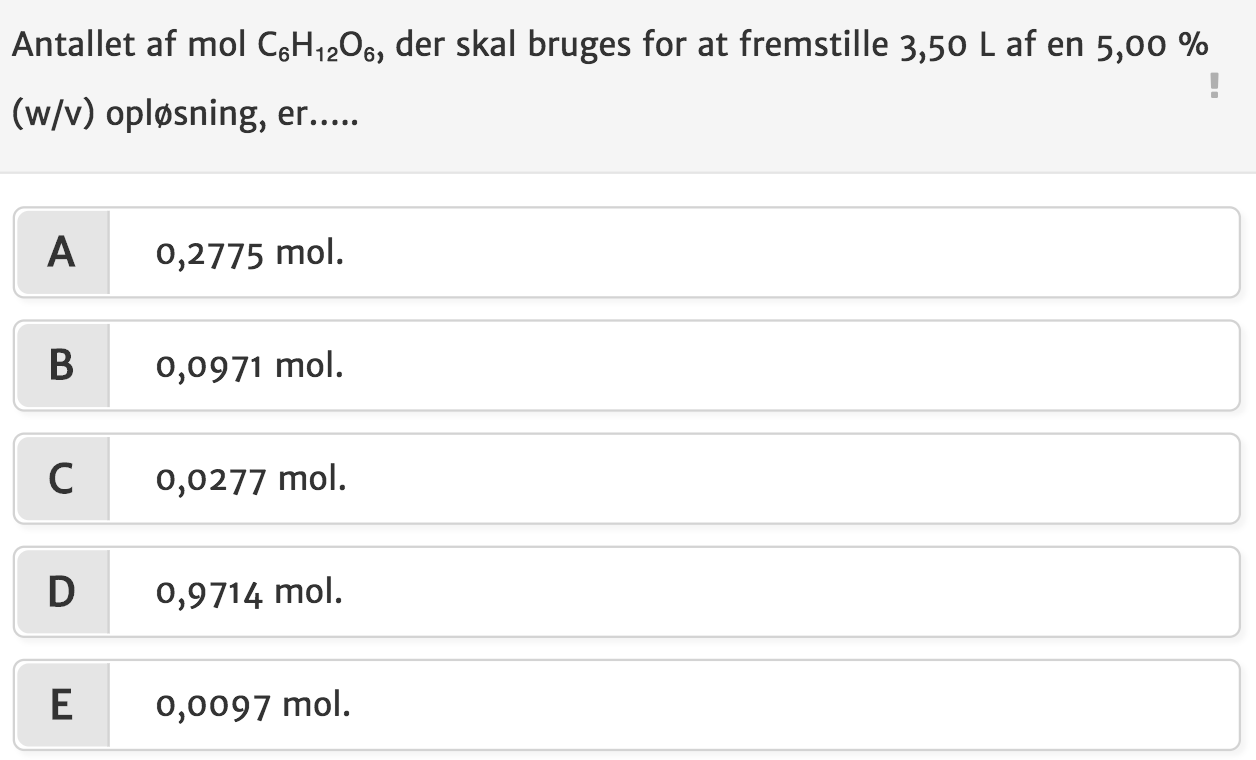
Finde antal mol (stofmængden) af et stof, der skal bruges for at fremstille 3,5 L af en 5,00 % (w/v) opløsning
25. december 2018 af
Egofaciens (Slettet)
-
Niveau: C-niveau
Jeg er ikke helt med på, hvordan jeg løser opgaven. Er det unødvendigt at beregne molarmassen fx? Fordi så kan man jo bruge formlen n =m/M, men så mangler man stadig at involvere de 3,5 L og de 5 %..
Vedhæftet fil: Skærmbillede 2018-12-25 kl. 15.48.38.png
Skriv et svar til: Finde antal mol (stofmængden) af et stof, der skal bruges for at fremstille 3,5 L af en 5,00 % (w/v) opløsning
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.